A. PERKEMBANGAN TEORI ATOM
1. Teori Atom Jonh Dalton
John Dalton mengemukakan hipotesa tentang atom berdasarkan hukum kekekalan massa (Lavoisier) dan hukum perbandingan tetap (Proust). Teori yang diusulkan Dalton:
- Atom merupakan bagian terkecil dari materi yang sudah tidak dapat dibagi lagi.
- Atom digambarkan sebagai bola pejal yang sangat kecil, suatu unsur memiliki atom-atom yang identik dan berbeda untuk unsur yang berbeda.
- Atom-atom bergabung membentuk senyawa dengan perbandingan bilangan bulat dan sederhana. Misalnya air terdiri atom-atom hidrogen dan atom-atom oksigen
- Reaksi kimia merupakan pemisahan atau penggabungan atau penyusunan kembali dari atom-atom, sehingga atom tidak dapat diciptakan atau dimusnahkan.
Kelemahannya adalah tidak menerangkan hubungan lautan senyawa dan daya hantar arus listrik, jika atom merupakan bagian terkecil dari suatu unsure dan tidak dapat dibagi lagi.
2. Teori Atom J.J Thomson
Setelah penemuan proton oleh Goldstein di tahun 1886 dan elektron oleh J.J. Thomson di tahun 1897. Kemudian pada tahun 1898 J.J Thomson mengemukakan model atomnya. Model atom Thomson menyatakan bahwa atom berbentuk bulat dimana muatan listrik positif yang tersebar merata dalam atom dinetralkan oleh elektron-elektron yang bermuatan negatif yang berada di antara muatan positif.
Model atom Thomson didasarkan pada asumsi bahwa massa elektron lebih kecil dari massa atom, dan elektron merupakan partikel penyusun atom. Karena atom bermuatan netral, maka elektron yang bermuatan negatif akan menetralkan suatu muatan positif dalam atom. Hal ini mendukung keberadaan proton dalam atom.
Kelebihan teori atom Thomson ini adalah membuktikan adanya partikel lain yang bermuatan negative dalam atom. Berarti atom bukan merupakan bagian terkecil dari suatu unsure. Selain itu juga memastikan bahwa atom tersusun dari partikel yang bermuatan positif dan negative untuk membentuk atom netral. Juga membuktikan electron terdapat dalam semua unsure.
Kelemahannya adalah belum dapat menerangkan bagaimana susunan muatan positif dalam bola dan jumlah electron
3. Teori Atom Rutherford
Eksperimen yang dilakukan Rutherford adalah penembakan lempeng tipis dengan partikel alpha. Ternyata partikel itu ada yang diteruskan, dibelokkan atau dipantulkan. Berarti di dalam atom terdapat susunan-susunan partikel bermuatan positif dan negatif.
Hasil penelitian Rutherford sekaligus menggantikan model atom Thomson, Rutherford mengajukakan model atom yang menyatakan bahwa atom tersusun dari inti yang bermuatan positif dikelilingi oleh elektron-elektron yang bermuatan negatif, seperti planet mengelilingi matahari.
Massa atom terpusat pada inti dan sebagian besar volum atom merupakan ruang hampa/kosong. Karena atom bersifat netral, maka jumlah muatan positif dalam inti (proton) harus sama dengan jumlah elektron.
Kelebihan teori atom Ritherford adalah menyatakan bahwa atom tersusun dari inti atom dan electron yang mengelilingi inti. Kelemahannya, model tersebut tidak dapat menerangkan mengapa electron tidak pernah jatuh ke inti sesuai dengan teori fisika klasik.
4. Model Atom Borh
Niels Bohr dengan percobaannya menganalisa spektrum warna dari atom hidrogen yang berbentuk garis. Hipotesis Bohr adalah :
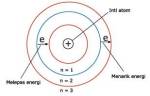
- Atom terdiri dari inti yang bermuatan positif dan dikelilingi oleh elektron yang bermuatan negatif di dalam suatu lintasan.
- Elektron dapat berpindah dari satu lintasan ke yang lain dengan menyerap atau memancarkan energi sehingga energi elektron atom itu tidak akan berkurang. Jika berpindah lintasan ke lintasan yang lebih tinggi maka elektron akan menyerap energi. Jika beralih ke lintasan yang lebih rendah maka akan memancarkan energi.
Kelemahan model atom ini adalah: tidak dapat menjelaskan spekrum warna dari atom berelektron banyak. Sehingga diperlukan model atom yang lebih sempurna dari model atom Bohr.






Tidak ada komentar:
Posting Komentar